Page 8 - MD Pulmonológia
P. 8
Beszámoló MD Pulmonológia 2022•1
Aktualitások a nem kissejtes szűkebb betegpopulációt beválogató
NADIM II elnevezésű, II. fázisú vizsgálat,
tüdőrák kezelésében amelyben 86, potenciálisan reszekálha-
tó, IIIA-B stádiumú beteget ran do mizáltak
2:1 arányban neoadjuváns nivolumab +
A Magyar Tüdőgyógyász Társaság Magyar Bronchológus Egyesületének kemoterápia és kemote rápiakarokra,
és Onkopulmonológiai Szekciójának konferenciája 2022. szeptember majd a műtét után az előbbi karon a
végén zajlott. A következőkben a rendezvény egyes előadásait nivolumabterápiát folytatták, míg a kont-
összefoglalva mutatjuk be a nem kissejtes tüdőrák (non-small cell lung rollkaron csak obszervációt alkalmaztak.
cancer, NSCLC) kezelését meghatározó legújabb klinikai vizsgálatokat, a A nivolumab + kemoterápia karon defi-
befogadott új indikációkat a korai stádium neoadjuváns és adjuváns, nitív műtéti ellátás a betegek 93%-ánál
illetve az előrehaladott betegség célzott terápiájában. történt, a kontrollkaron ez 69% volt; az
elsődleges végpont pCR-t pedig a nivolu-
mab + kemoterápia karon még maga-
sabbnak találták, mint a CheckMate
816-vizsgálatban (36,8%).
NEOADJUVÁNS ÉS free survival, EFS) szignifikánsan jobb Az első, Európai Gyógyszerügy nökség
ADJUVÁNS KEZELÉSEK eredményt mutattak a nivolumabot is (EMA) által befogadott adju váns
KORAI NSCLC-BEN kapó betegcsoportban: a patológiai immunellenőrzőpontgátló-ke zelés befo-
komplett válasz (pCR) aránya 24% vs. gadásához az IMpower010-vizs gálat
sárosi VeronikA és rojkó líViA 2,2%, az mEFS 31,6 vs. 20,8 hónap eredményei vezettek. Ebben IB-IIIA stádi-
előAdásAi AlApján volt. Fontos megemlíteni, hogy a pCR-t umú, komplett reszekción átesett betegek
A korai stádiumú nem kissejtes tüdőrák elérő betegeknél az EFS-re vonatkozó (n=1005) kaptak kötelező jelleggel adju-
kiújulásának aránya még komplett esélyhányados igen magas (0,13) volt a vánsan cisplatinalapú kemoterápiát,
reszekció esetén is magas: az elkóborolt pCR-t el nem érőkhöz viszonyítva (0,84). majd 1:1 arányú rando mizáció után egy
mikrometasztázisok későbbi aktiválódá- Az amerikai Élelmiszer- és Gyógy- évig atezolizumabot, illetve szupportív
sa miatt a betegek akár 60%-ában reci- szerfelügyeleti Hatóság (FDA) a vizsgálat ellátást (best sup portive care, BSC). A
dívára számíthatunk, amely az esetek eredményei alapján 2022 ben befogad- PD-L1 ≥1% populációban az elsődleges
60-80%-ában távoli áttét formájában ta a nivolumabot platinaalapú kemote- végpont, a betegségmentes túlélés
jelentkezik. Ezt igyekszünk megakadá- rápiával kombinálva a korai NSCLC (disease-free survival, DFS) lényegesen
lyozni a neoadjuváns és adjuváns keze- neoadjuváns kezelésébe. magasabb volt az atezolizumabkaron (3
lésekkel: a citotoxikus kemoterápiával a Ugyancsak a neoadjuváns immun- éves DFS-arány 60% vs. 48%; HR: 0,66),
keringő tumorsejteket próbáljuk elpusztí- kemoterápia eredményességét igazolja a hasonlóan a teljes túléléshez (5 éves
tani, míg az immunterápia a T-sejtek
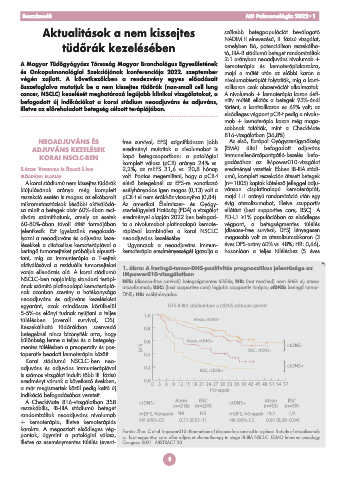
aktiválásával a reziduális tumor sejteket 1. ábra: A keringő-tumor-DNS-pozitivitás prognosztikus jelentősége az
vonja ellenőrzés alá. A korai stádiumú IMpower010-vizsgálatban
NSCLC-ben napjainkig standard terápi- DFS: (disease-free survival) betegségmentes túlélés; NR: (not reached) nem érték el; atezo:
ának számító platinaalapú kemoterápiá- atezolizumab; BSC: (best supportive care) legjobb szupportív terápia; ctDNS: keringő tumor-
nak azonban szerény a hatékonysága DNS; HR: esélyhányados
neoadjuváns és adjuváns kezelésként
egyaránt, azok mindössze körülbelül
5-5%-os előnyt tudnak nyújtani a teljes
túlélésben (overall survival, OS).
Re szekál ható tüdőrákban szenvedő
betegeknél nincs bizonyíték arra, hogy
különbség lenne a teljes és a betegség-
mentes túlélésben a preoperatív és pos-
toperatív beadott kemoterápia között.
Korai stádiumú NSCLC-ben neo-
adjuváns és adjuváns immunterápiával
is számos vizsgálat indult: több III. fázisú
eredményt várunk a következő években,
a már megismertek közül pedig kettő új
indikáció befogadásához vezetett.
A CheckMate 816-vizsgálatban 358
reszekábilis, IB-IIIA stádiumú beteget
randomizáltak neoadjuváns nivolumab
+ kemoterápia, illetve kemoterápiás
karokra. A megosztott elsődleges vég- Forrás: Zhou C et al. Impower010: Biomarkers of disease-free survival in a phase 3 study of atezolizumab
pontok, úgymint a patológiai válasz, vs. best supportive care after adjuvant chemotherapy in stage IB-IIIA NSCLC. ESMO Immono-oncology
illetve az eseménymentes túlélés (event- Congress 2021. ABSTRACT 20
8