Page 19 - Dermatology Times 4. szám
P. 19
ÁLTALÁNOS BŐRGYÓGYÁSZAT
DECEMBER 2020 ⁄ DERMATOLOGIA.OLO.HU 19
®
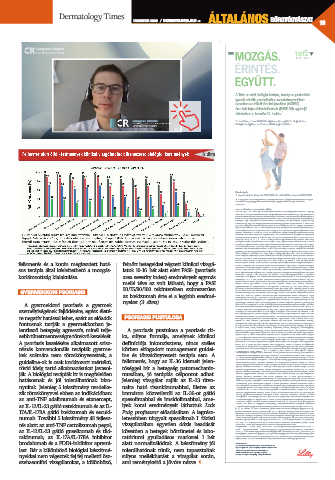
A Taltz az első biológiai terápia, amely szuperioritást
igazolt arthritis psoriaticában az adalimumabbal*
szemben az ízületi tünetek javulása (ACR50)
és a bőr teljes feltisztulásának (PASI100) egyidejű
elérésében a kezelés 24. hetén. 1
*a korábban ≥1 csDMARD terápiára nem reagáló és megelőzően
biológiai terápiában nem részesülő betegek körében 1
3. ábra
Hivatkozások:
1. Mease PJ, et al. Ann Rheum Dis 2020;79:123–131. doi:10.1136/annrheumdis-2019-215386
▼ Ez a gyógyszer fokozott felügyelet alatt áll, mely lehetővé teszi az új gyógyszerbiztonsági információk gyors
azonosítását. Az egészségügyi szakembereket arra kérjük, hogy jelentsenek bármilyen feltételezett
mellékhatást.
TALTZ▼ RÖVIDÍTETT ALKALMAZÁSI ELŐÍRÁS
TALTZ 80 mg / 1 ml oldatos inj. előretöltött injekciós tollban. A hatóanyag neve ixekizumab, mely egy
rekombináns humanizált monoklonális antitest. Terápiás javallat: A Taltz közepesen súlyos vagy súlyos plakkos
psoriasis kezelésére javallott szisztémás kezelésre szoruló felnőtteknél, valamint szisztémás kezelésre szoruló ≥
6 éves és ≥ 25 kg testtömegű gyermekek és serdülőknél. A Taltz az aktív arthritis psoriatica kezelésére javallott
önmagában vagy metotrexáttal kombinálva azoknál a felnőtteknél, akik nem reagáltak megfelelően vagy
intoleránsak egy vagy több betegségmódosító rheumaellenes gyógyszerrel végzett kezelésre. A Taltz az aktív
spondylitis ankylopoetica kezelésére javallott azoknál a felnőtt betegeknél, akik nem reagáltak megfelelően a
hagyományos kezelésre. A Taltz az aktív nem radiológiai axiális spondyloarthritis kezelésére javallott azoknál a
felnőtt betegeknél, akiknél a megemelkedett CRP és/vagy az MRI objektíven jelzi a gyulladás jelenlétét, és nem
reagáltak megfelelően a NSAID-okra. A Taltz az indikációkban szereplő betegségek diagnosztizálásában és
kezelésében jártas orvos vezetése és felügyelete alatt történő alkalmazásra való. Adagolás és alkalmazás:
Plakkos psoriasisban felnőtteknél az ajánlott adag 160 mg, subcutan injekcióban (két 80 mg-os injekció) a 0.
héten, majd 80 mg a 2., 4., 6., 8., 10. és 12. héten, ezután 80 mg-os fenntartó adag minden 4. héten. 50 kg
feletti gyermek esetén a javasolt kezdő dózis 160 mg a 0. héten, majd ezt követően 4-hetente 80 mg. A Taltz 80
mg előretöltött injekciós toll csak azoknál a gyermekeknél használható, akiknek 80 mg-os adagra van szükségük
a dózis előkészítése nélkül. A 25-50 kg testtömegű gyermekek kezelésére a Taltz más gyógyszerformája (az
előretöltött injekciós fecskendő) használható, és a 80 mg-nál alacsonyabb dózisokat, amelyek külön elkészítést
igényelnek, csak egészségügyi szakember adhatja be. Arthritis psoriaticaban az ajánlott adag 160 mg, subcutan
injekcióban (két 80 mg-os injekció) a 0. héten, majd 80 mg (egy injekció) minden 4. héten. Arthritis psoriatica
mellett közepesen súlyos/súlyos plakkos psoriasisban is szenvedő betegeknél a plakkos psoriasisra vonatkozó
adagolási rend javasolt. Axiális spondyloarthritisben (radiológiai és nem radiológiai) az ajánlott adag 160 mg,
subcutan injekcióban (két 80 mg-os injekció) a 0. héten, majd 80 mg minden 4. héten. Az összes javallat
felismerés és a korán megkezdett hatá- felnőtt betegekkel végzett klinikai vizsgá- esetében (plakkos psoriasis, arthritis psoriatica, axiális spondyloarthritis) a kezelés abbahagyása mérlegelendő
azoknál a betegeknél, akik 16-20 hetes kezelés után nem mutatnak terápiás választ. A kezdetben részleges
sos terápia által késleltethető a mozgás- latok 10-16. hét alatt elért PASI- (psoriasis válaszreakciót mutató egyes betegek a kezelés 20. hét utáni folytatásakor további javulást mutathatnak. A Taltzot
subcutan injekcióként kell beadni, a beadási hely változtatható, a psoriasisos bőrterületeket lehetőleg kerülni
kell. Az injekciós technika elsajátítása után a betegek maguknak is beadhatják a készítményt (kivéve a 80 mg-nál
korlátozottság kialakulása. area severity index) eredményeit egymás alacsonyabb dózisokat). A Taltz alkalmazása nem javasolt < 25 kg testtömegű gyermekeknél. A gyermekek
testtömegét fel kell jegyezni, és a kezelések előtt rendszeresen ellenőrizni kell. A Taltz biztonságosságát és
hatásosságát 2 - < 18 éves, arthritis psoriaticában szenvedő gyermekek és serdülők esetében még nem
mellé téve az volt látható, hogy a PASI igazolták. 6 évesnél fiatalabb gyermekeknél a közepesen súlyos vagy súlyos plakkos psoriasis indikáció, illetve 2
évesnél fiatalabb gyermekeknél arthritis psoriatica indikáció esetén nincs releváns alkalmazás.
Figyelmeztetések és ellenjavallatok: A Taltz-kezeléshez a fertőzések, (pl. felső légúti fertőzés, oralis
50/75/90/100 tekintetében számszerűen candidiasis, conjunctivitis és gombás bőrfertőzések) fokozott gyakorisága társul. Klinikailag jelentős krónikus
GYERMEKKORI PSORIASIS fertőzés esetén a Taltz csak óvatosan alkalmazható. Fertőzés kialakulása esetén, ha az súlyos vagy a szokásos
kezelésre nem reagál, akkor a Taltz-kezelést abba kell hagyni. Aktív TBC-ben szenvedő betegeknek nem szabad
az ixekizumab érte el a legjobb eredmé- Taltzot adni. Látens TBC esetén a Taltz elkezdése előtt antituberkulotikus kezelés mérlegelendő. Súlyos
túlérzékenységi reakciókat, (pl. angiooedema, urticaria) jelentettek, akár késői reakcióként is. Ilyenkor a Taltz
nyeket (3. ábra). adagolását azonnal fel kell függeszteni, és megfelelő kezelést kell elkezdeni. Az ixekizumabbal vagy bármely
segédanyaggal szembeni súlyos túlérzékenység esetén a kezelés ellenjavallt. Gyulladásos bélbetegségek
A gyermekkori psoriasis a gyermek (ideértve a Crohn-betegséget és a colitis ulcerosát) új eseteinek kialakulásáról vagy exacerbatiójáról számoltak
be az ixekizumabbal kapcsolatban; ilyen betegségben szenvedőknél az ixekizumab alkalmazása nem ajánlott. Ha
személyiségének fejlődésére, egész életé- a betegnél gyulladásos bélbetegség alakul ki, vagy a már meglévő gyulladásos bélbetegség exacerbatióját
tapasztalják, az ixekizumab-kezelést abba kell hagyni, és megfelelő orvosi kezelést kell elkezdeni. A Taltz
biztonságosságát plakkos psoriasisban egyéb immunmodulánsokkal vagy fototerápiával végzett kombinált
re negatív hatással lehet, ezért az előadók PSORIASIS PUSTULOSA kezelésben nem értékelték. Nem észleltek kölcsönhatást, ha a Taltzot metotrexáttal és/vagy kortikoszteroidokkal
adták együtt arthritis psoriaticában szenvedő betegeknek. Fogamzóképes nőknek a kezelés alatt és utána
fontosnak tartják a gyermekkorban je- legalább 10 hétig hatékony fogamzásgátló módszert kell alkalmazniuk. Nemkívánatos hatások,
mellékhatások: Nagyon gyakori (>10%): felső légúti fertőzések, reakció az injekció beadásának helyén. Gyakori
(1-10%): gombás bőrfertőzés, mucocutan herpes simplex, oropharyngealis fájdalom, hányinger. Nem gyakori
lentkező betegség agresszív, minél telje- A psoriasis pustulosa a psoriasis rit- (0,1-1%): influenza, rhinitis, szájüregi candidiasis, conjunctivitis, cellulitis, neutropenia, thrombocytopenia,
angiooedema, gyulladásos bélbetegség, urticaria, bőrkiütés, ekzema. Ritka: (0,01-0,1%) anaphylaxia. Az injekció
beadásának helyén leggyakrabban erythemát és fájdalmat jeleztek, és túlnyomórészt enyhék vagy közepesen
sebb tünetmentességre törekvő kezelését. ka, súlyos formája, amelynek klinikai súlyosak voltak. A Taltzcal kezelt plakkos psoriasisos felnőtt betegekben 12 hét kezelés során a betegek
27,2%-ánál jelentették fertőzés kialakulását, melyből 0,6 % volt súlyos. A teljes kezelési időszakban a betegek
52,8%-ánál jelentettek fertőzést (46,9/100 betegév), melyből súlyos 1,6% (1,5/100 betegév). Az arthritis
A psoriasis kezelésére alkalmazott szisz- definíciója inkonzisztens, nincs széles psoriaticában és az axiális spondyloarthritisben végzett klinikai vizsgálatokban megfigyelt infekciók gyakorisága
hasonló volt a plakkos psoriasis vizsgálata során megfigyelthez, kivéve az influenza és conjunctivitis
mellékhatásokat, amelyek az arthritis psoriaticában szenvedő betegeknél gyakoriak voltak. Plakkos psoriasisban
témás konvencionális terápiák gyerme- körben elfogadott management guidel- Taltz-kezelés alatt a kontroll labor vizsgálatok során a betegek 9%-ánál alakult ki neutropenia, a legtöbb esetben
a neutrophilszám ≥1000 sejt/mm 3 volt. A betegek 0,1%-ánál alakult ki <1000 sejt/mm 3 sejtszám.
kek számára nem törzs könyvezettek, a ine és törzskönyvezett terápia sem. A Thrombocytopenia a betegek 3%-ánál jelentkezett. Arthritis psoriaticában és az axiális spondyloarthritisben a
neutropenia és thrombocytopenia gyakorisága hasonló volt. A Taltz-kezelésben részesülő felnőtt betegek kb.
9-17%-ánál képződtek gyógyszerellenes antitestek, amelyek többségénél az antitesttiter alacsony volt, és nem
guideline-ok is csak korlátozott mértékű, felismerés, hogy az IL-36 kiemelt jelen- járt csökkent klinikai válasszal. A betegek kb. 1%-ában igazoltak alacsony gyógyszerkoncentrációval és csökkent
klinikai válaszreakcióval járó neutralizáló antitesteket. Arthritis psoriaticában szenvedő betegek kb. 11%-ánál
rövid ideig tartó alkalmazásukat javasol- tőséggel bír a betegség patomechaniz- képződtek gyógyszerellenes antitestek, amelyek többségénél az antitest-titer alacsony volt, és körülbelül 8%-ánál
igazoltak neutralizáló antitesteket. A radiológiai axiális spondyloarthritisben szenvedő betegek 5,2%-ánál
képződtek gyógyszerellenes antitestek, amelyek többségénél az antitest-titer alacsony volt, és 1,5%-ánál
ják. A biológiai terápiák itt is megfelelően musában, jó terápiás célpontot adhat. igazoltak neutralizáló antitesteket. A nem radiológiai axiális spondyloarthritisben szenvedő betegek 8,9%-ánál
képződtek gyógyszerellenes antitestek, az antitest-titer minden esetben alacsony volt, egyik betegnél sem
igazoltak neutralizáló antitesteket. Sem arthritis psoriatican sem az axialis spondyloarthritisben a
hatásosnak és jól tolerálhatónak bizo- Jelenleg vizsgálat zajlik az IL-23 útvo- gyógyszerellenes antitestek, a gyógyszerkoncentráció, a hatásosság vagy a biztonságosság között nem lehetett
nyilvánvaló kapcsolatot megfigyelni. A Taltz-cal kezelt, plakkos psoriasisban szenvedő gyermekeknél megfigyelt
biztonságossági profil összességében megfelelt a plakkos psoriasisban szenvedő felnőttekével, kivéve a
nyultak. Jelenleg 5 készítmény rendelke- nalra ható risankizumabbal, illetve az kötőhártya gyulladás, influenza és az urticaria előfordulási gyakoriságát, amelyek gyakoriak voltak. A gyulladásos
bélbetegség is gyakoribb volt a gyermekeknél, de még így is a nem gyakori kategóriába tartozott. Az ajánlott
zik törzs könyvvel ebben az indikációban: immáron közvetlenül az IL-36-ot gátló dozírozásban max. 12 héten át Taltz-cal kezelt gyermekkori psoriasisban szenvedő betegek közül 18%-nál
képződtek gyógyszerellenes antitestek, közülük a felénél az antitest-titer alacsony volt, és 4%-nál igazoltak
alacsony gyógyszerkoncentrációkkal kapcsolatba hozható neutralizáló antitesteket. Tárolás: Az eredeti
az anti-TNF adalimumab és etanercept, spesolimabbal és imsidolimabbal, ame- csomagolásban, hűtőszekrényben (2°C – 8°C) tárolandó nem fagyasztható! A Taltz hűtés nélkül legfeljebb 30°C
hőmérsékleten legfeljebb 5 napig tárolható. A Taltz 80 mg oldatos injekció előretöltött injekciós toll használatát
a dobozban mellékelt Használati útmutató részletesen tartalmazza. Az alkalmazási előírás jóváhagyásának
az IL-12/IL-23 gátló ustekinumab és az IL- lyek korai eredményeit láthattuk Luis dátuma: 2020. június 26. Gyógyszer kiadhatósága, társadalombiztosítási támogatás feltétele és
mértéke 1 : az egészségügyi szakellátás társadalombiztosítási finanszírozásának egyes kérdéseiről szóló 9/1993.
(IV. 2.) NM rendelet 1/A. számú mellékletének (Tételes elszámolás alá eső hatóanyagok jegyzéke és kódja,
17A/IL-17RA gátló ixekizumab és secuki- Puig professzor előadásában. A legrész- indikációs területek és a felírásra jogosultak köre) 4. és 5. pontja alapján arthritis psoriatica és plakkos psoriasis
indikációkban tételes finanszírozásban részesül a rendelet mellékletében 1 meghatározott indikációs és felírói
numab. További 5 készítmény áll fejlesz- letesebben tárgyalt spesolimab I. fázisú körben. Kiadhatóság 2 : vényköteles, a szakorvosi/kórházi diagnózist követően folyamatos szakorvosi ellenőrzés
mellett alkalmazható gyógyszer (SZ),▼Fokozott felügyelet alatt álló gyógyszer. Ár 3 : Taltz 80 mg oldatos injekció
előretöltött injekciós tollban 1x bruttó fogyasztói ára: 302.390, - Ft, TB támogatás összege: 0, - Ft, térítési díj:
tés alatt: az anti-TNF certolizumab pegol, vizsgálatában egyetlen dózis beadását 302. 390, - Ft. A tételes elszámolás alá eső készítményeket a finanszírozó természetben biztosítja. További
információért, bővebb tájékoztatásért kérjük olvassa el a részletes alkalmazási előírást.
Hivatkozások: 1. 9/1993. (IV.2.) NM rendelet: https://net.jogtar.hu/jogszabaly?docid=99300009.NM, 2.
az IL-12/IL-23 gátló guselkumab és tild- követően a betegek bőrtünetei és labo- OGYÉI Gyógyszeradatbázis: https://www.ogyei.gov.hu/gyogyszeradatbazis&action=show_details&item=
143181, 3. NEAK Publikus Gyógyszertörzs – lakossági tájékoztató: http://neak.gov.hu/felso_menu/szakmai_ol-
rakizumab, az IL-17A/IL-17RA inhibitor ratóriumi gyulladásos markerei 1 hét dalak/gyogyszer_segedeszkoz_gyogyfurdo_ tamogatas/egeszsegugyi_vallalkozasoknak/pupha/Vegleges_PUP-
HA.html A feltüntetett árat és a támogatás mértékét a 2020.07.08-án a neak.gov.hu oldalon hozzáférhető adatok
alapján közöltük, az aktuális árak tekintetében kérjük ellenőrizze a NEAK Publikus gyógyszertörzsét.
brodalumab és a PDE4-inhibitor apremi- alatt normalizálódtak. A készítmény jól PP-IX-HU-0178
A dokumentum zárásának dátuma: 2020. november 17.
last. Bár a különböző biológiai készítmé- tolerálhatónak tűnik, nem tapasztaltak Lilly Hungária Kft. 1075 Budapest, Madách Imre út 13-14.,
Tel: (1)3285100 Fax: (1)3285101 www.lilly.hu
Taltz is a trademark of Eli Lilly and Company.
nyekkel nem végeztek fej fej melletti ösz- súlyos mellékhatást a vizsgálat során, © 2020 Eli Lilly and Company. All rights reserved.
szehasonlító vizsgálatokat, a különböző, ami reménykeltő a jövőre nézve.